
内毒素(Endotoxin)是一种脂多糖(LPS),来源于革兰氏阴性细菌外膜,其细胞壁外膜的外部脂质成分由内毒素分子组成,细胞死亡或分解后被释放出来。内毒素单位为EU。
当内毒素进入血液或CSF(脑脊液)时会引起发热,也称为热原。因此必须从药品、注射用生物制剂和一些组织培养培养基中去除。
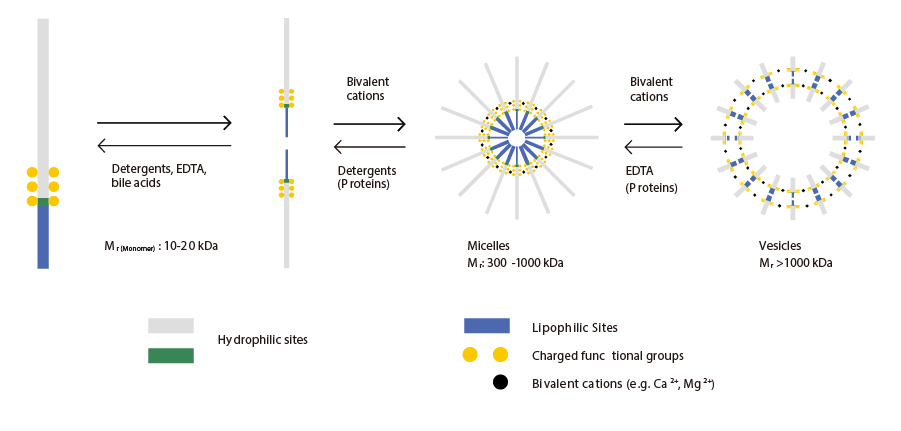
图1:不同组成的水溶液中内毒素聚集体的结构
图1 显示,溶液中的内毒素单体分子量在10 ~ 20 kDa之间,但它们可以形成直径达0.1μm的胶束和囊泡。洗涤剂、螯合剂和蛋白质的存在促进胶束(300-1000kDa) 和单体 (10-20kDa) 等结构的形成,而二价离子促进囊泡(>1000 kDa) 等大结构的形成。如果待去热原溶液中的目标物质分子量小(如缓冲液、盐、核苷酸、氨基酸、肽、一些碳水化合物等),内毒素可以用适当的切向流膜包进行超滤,从目标物质中分离出来。然而,与内毒素在相同分子量范围内的蛋白质不能通过超滤的方式分离。
由于内毒素中含有带负电荷的磷酸基和羧基,内毒素单体等电点在2左右,相对较低,即在pH>2的溶液中内毒素表现出电负性,所以离子交换层析法是常用除去热源的方法之一。
而由于传统填料的层析方法存在一些缺点,这些缺点限制了它作为除内毒素步骤的应用。这里面包括操作和使用问题,如填料的湍流、流速低、操作繁琐、再生时间长和有限的化学稳定性等。低流速和对污垢的敏感性意味着将层析填料纳入大规模生产的纯化步骤可能是麻烦和昂贵的。
科百特推出了高容量、可扩展和即用型离子交换膜吸附器(层析)技术,该膜吸附器(层析)的流速快,载量大,满足了在实验室或工艺规模中除热源所需的优异性能。

在为含有蛋白质和多肽的介质或溶液设计去热原方案时,需要考虑许多因素:目标物质类型、蛋白质或多肽、产物浓度、分子量和等电点(pI); 溶液电导; pH值和缓冲系统; 以及相互作用,比如干涉或聚集。一般来说,这些因素决定了最终能否有效的去除热原。
使用Q强阴离子膜交换吸附器(层析)和pH低于蛋白质pl的缓冲液,内毒素被膜吸附,而目标产品将透过膜被收集。
内毒素的去除用log降低值(LRV)表示

阴离子交换流穿纯化步骤中的除内毒素研究
虽然Q膜对内毒素载量>106EU/ml即 1ml Q膜能负载总量106EU以上的内毒素,载量较高。但在实际生物制药应用中初始料液内毒浓度大多低于100EU/ml,对除内毒后料液中内毒素含量标准较高,一般要求<0.25EU/ml,因此在实际应用中,更关注Q膜能将内毒素降低至多少水平。(即更关注在料液中内毒素低负载时的LRV值)。
本研究在低负载条件下使用DOE实验对Q膜在去除制剂Buffer中内毒素的性能进行研究
经前期筛选评估,最终选择pH、NaCl、蔗糖浓度三因子进行DOE实验(Box-Behnken设计)
因子A:pH;设计空间范围 4 ~ 9;
因子B:蔗糖浓度(W/V);设计空间范围 0 ~ 15 %;
因子C:NaCl浓度(mM);设计空间范围 0 ~ 200 mM;
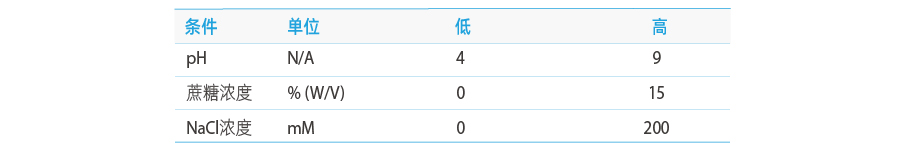
设置5个中心点
共生成17组实验,如下表所示mM
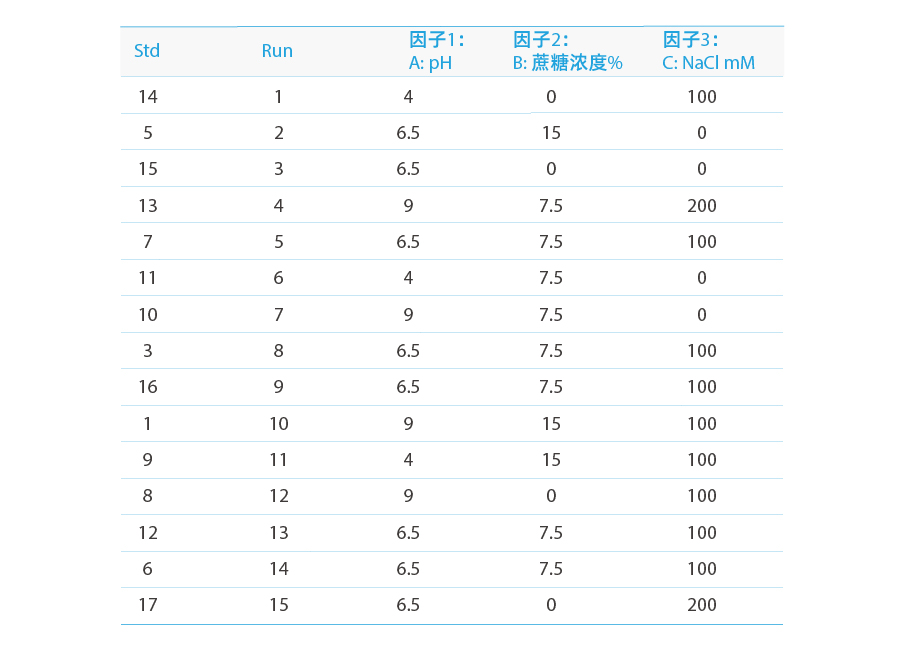
实验方法
测试溶液加标内毒素浓度:100 EU/ml
Purcise™ Q 膜体积:0.9 ml (16层膜配置)
Purcise™ Q 膜过滤加标溶液体积:90 ml
过滤流速:9 ml/min (10 MV/min)
收集Q膜滤前、滤后液,取样测内毒素浓度
内毒素的去除用log降低值(LRV)表示。
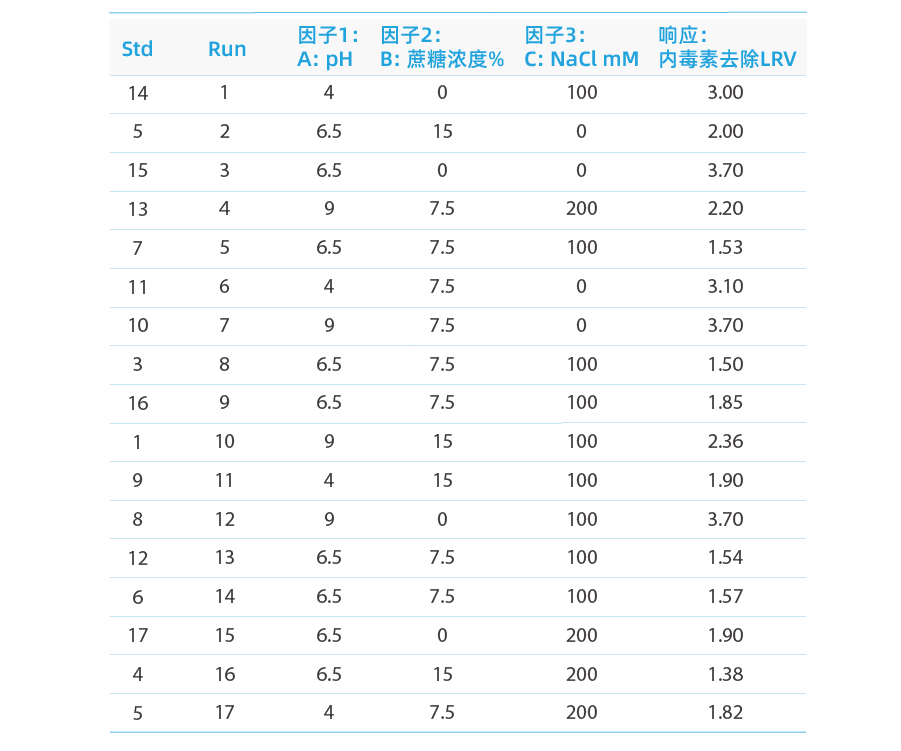
根据软件进行统计学分析结果如下:
响应: 内毒素去除LRV值
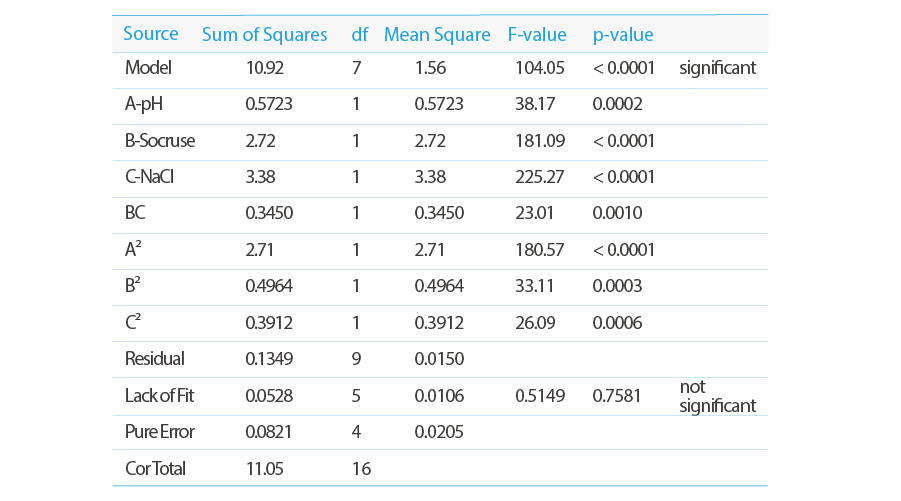
Model F-value 为104.05表示模型显著
P-values小于0.05表示模型项显著。
在这种情况下,A、B、C、BC、A²、B²、C²是重要的模型项
Lack of Fit F-value 为0.51意味着失拟相对于纯误差不显著
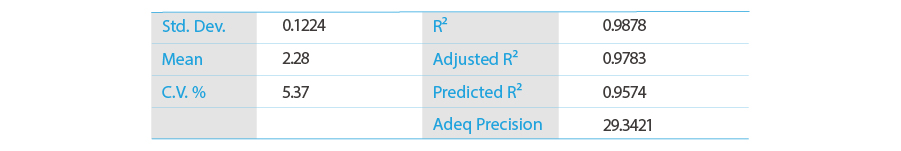
统计量
拟合模型最终方程

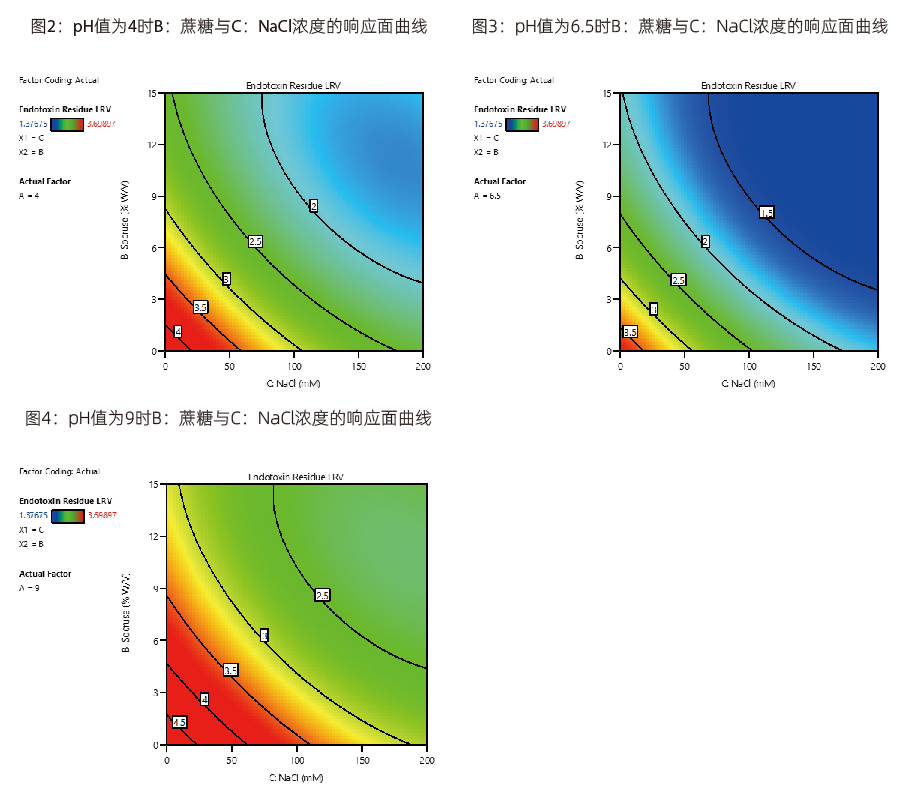
响应面曲线图
验证实验 I
测试溶液配方:50 mM Tris,50 mM NaCl,9% 蔗糖,pH7.5
测试溶液加标内毒素浓度:43.8 EU/ml
Purcise™ Q膜体积:0.9 ml(16层膜配置)
Purcise™ Q膜过滤加标溶液体积:300 ml
过滤流速:9 ml/min(10 MV/min)
收集Q膜滤前、滤后液,取样测内毒素浓度
结果显示使用Purcise™ Q膜过滤300 ml内毒浓度为43.8 EU/ml的制剂Buffer,滤后内毒<0.12 EU/ml(凝胶法测定),符合模型计算预期。压力由初始8.7 psi上升至9.72 psi。
验证实验 II
测试溶液配方:50 mM Tris,9% 蔗糖,pH7.2
测试溶液加标内毒素浓度:16.11 EU/ml
Purcise™ Q膜体积:0.45 ml(8层膜配置)
Purcise™ Q膜过滤加标溶液体积:1500 ml
过滤流速:9 ml/min(20 MV/min)
收集Q膜滤前、滤后液,取样测内毒素浓度
结果显示使用Purcise™ Q膜过滤1500 ml内毒浓度为16.11 EU/ml的制剂Buffer,滤后内毒为0.024 EU/ml(动态显色法测定),符合模型计算预期。
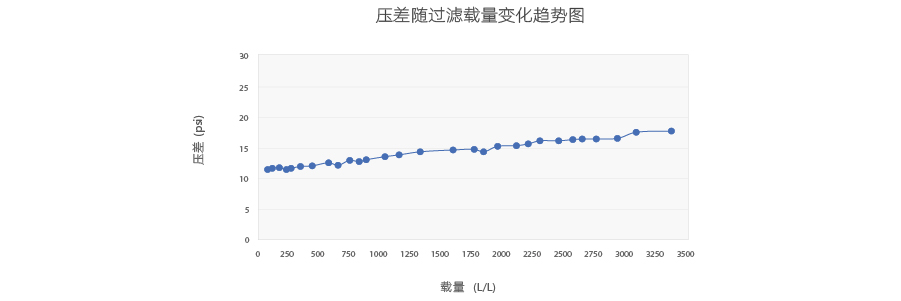
Purcise™ Q 0.45ml(8层配置)载量压力曲线
结 论
在低负载条件下,Purcise Q在内毒素清除中pH、蔗糖浓度、NaCl浓度条件均对最终内毒素清除存在显著影响(P<0.05)。其中NaCl浓度和蔗糖浓度对Purcise™ Q膜去除内毒素效果有交互效应。
经实验验证的Purcise™ Q膜在低负载条件下去除内毒素的DOE拟合数学模型实际可用,数学模型为:
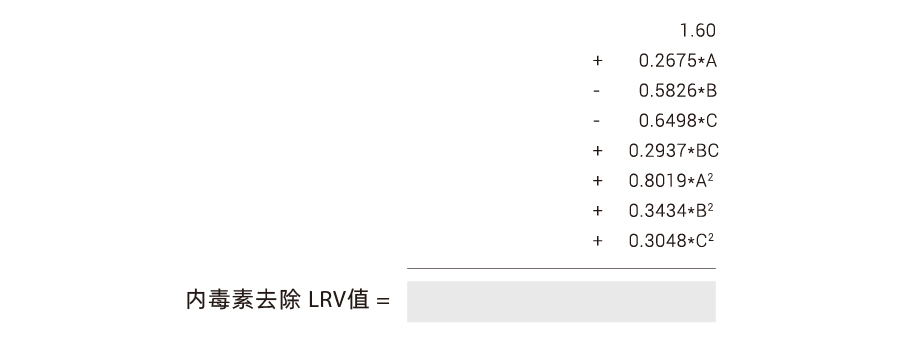
A:pH值
B:蔗糖浓度
C:NaCl浓度
在低负载条件下Purcise™ Q膜在合适的pH、盐浓度条件下除内毒能力能达到LRV>3。可以根据实际料液组成带入模型公式计算最终Purcise™ Q膜除内毒LRV值
推荐Q膜除内毒条件范围:pH:4 ~ 9, 蔗糖浓度(W/V):0 ~ 9%,NaCl(mM):0 ~ 50 mM
8层Purcise™ Q膜在除内毒性能上与16层Purcise™ Q膜基本一致,8层Purcise™ Q膜过滤压差较低,流速更快(推荐流速1 ~ 25 MV/min,最大耐压3 bar),能在高粘度物料上保证稳定流速。




